TOPICS
コールドチェーン
凍結細胞の効果を最大化する
凍結細胞の効果を最大化する
Maximizing the Efficacy of Cryopreserved Cellular Therapies.
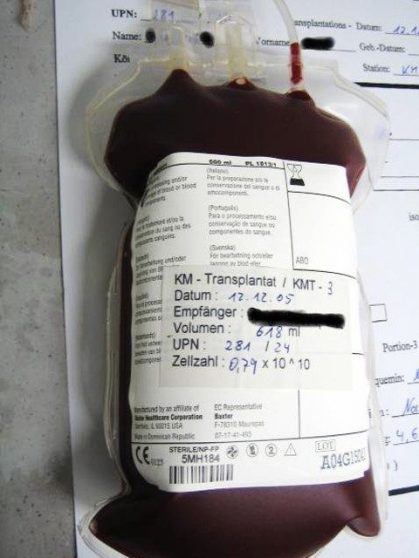
血液由来の幹細胞は、大抵の場合移植前に凍結保存が行われます。(出展:Wikipedia)
*Astero Bio社が旧medcision社の事業を承継しておりましたが、Astero Bio社がBioLife Solutions社に吸収合併されたことにより、現在はBioLife Solutions社が事業を引き継いでいます。
細胞療法は、医療産業として最大級の期待が寄せられています。すでにFDAの承認を得ている新しい製品も幾つかあります。例えば、幹細胞移植に使用される臍帯血療法のALLOCORDや、生細胞ワクチンで、前立腺がんに使用されるDendreon社のPROVENGEがあります。従来の臍帯血輸血から間葉系幹細胞療法、新しいがん免疫療法など、細胞療法の臨床試験は、ますます増加しているところです。
これら新しい治療法の創造性に目を奪われ、その先のことが考えられなくなりがちです。特定の種類のがん細胞を攻撃するよう、患者自身の免疫細胞を操作することや、成人細胞から直接多能性幹細胞を作り出せるようになると、10年前に誰が考えたでしょうか。
しかし、難しい問題は細部にあります。ここでいう細部とは、最終的には患者の治療効果を決定する細胞の輸送であったり、凍結、融解、注入などささいなものを指します。実験的な生細胞療法から、安全で有効な治療への転換は、さらなる効率性の構築や、患者のリスク最小化、治療有効性を最大化するなどの、イノベーションが関連する長いプロセスです。自身に由来する細胞であっても、適切な方法や予防措置が無い状態で再導入することは、絶対に安全というわけではありませんし、体から細胞を採取する際には、自身の組織サンプルや、そのプロセス中に使用された装置から、他種の細胞や病原体によるコンタミの可能性が常にあります。凍結保存、融解、洗浄ステップなど、単純に思えるプロセスでも、その操作が細胞にダメージを与えたり、機能に変化をもたらすことがあります。
この問題においては、細胞に対するリスクを回避するよう、上記のプロセスを標準化し、最適化しなければなりません。
今日、米国FDAによって承認されている細胞療法のうち、白血病やその他の血液疾患に適応した、造血幹細胞をベースとした製品が大半を占めています。現代の細胞培養の創成期であった1956年に、ヒトの骨髄移植が初めて成功したことを考えれば、驚くことではありません。しかし、このよく認知された療法でも、一部は研究段階にあります。生着成功率は、様々な要素に影響を受けますが、最も重要なものの一つが、幹細胞の凍結、融解に使用される方法です。
ミラノの臍帯血バンクの研究者が行った最近のレビュー[1]で、現在利用されている造血幹細胞の凍結保存、融解方法を刷新することを求めています。この研究チームは、臍帯血産業は、長い経験があるにも関わらず、凍結保存や保管、融解方法でコンセンサスが得られておらず、プロトコルや品質管理法の作成、実行は各々の研究室任せの状態であり、生着の成功率という点においては、結果にばらつきがあると述べています。
凍結保存のプロセスにおける重要なコントロールポイントを定義することが重要であるとしています。この重要なコントロールポイントが製品の有効性や安全性の決定に最も寄与するためです。これらのプロセスで最も重要なことは、バリデーション、つまり、臍帯血サンプルの識別が妥当かの検証、そして、そのプロセスの全ポイントで細胞が曝露する環境の検証を正確に行うことです。
すなわち、ラベリングや品質管理、特に温度コントロールや処理プロセスを通しての追跡など、厳密なケアを行うということです。
当該研究チームは、移植に最適な品質を確保するには、凍結液を加える前と後、そして融解後に採集を行い、有核細胞を計数するよう推奨しています。凍結液の各々の成分についても、厳密に定義すべきです。特にDMSOに関しては、融解後の細胞生存率のため、濃度が適切になるよう検証を行います。
研究チームはまた、研究室や患者のベッドサイドで融解を行うことについて、それぞれの利点と欠点を評価しています。
現状の融解方法は標準化に欠けており、準最適な融解環境が、移植後の副反応につながる可能性があります。
融解後の生存率は生着率の大きな指標であり、不均一な融解は、下流の機能にダメージを与えるおそれがあります。患者への投与に先だって、例えば製品の輸送中や保管中に、細胞を不用意に温度上昇させないことが重要です。[1,2]しかし、凍結保存細胞の融解後の高い生存率が、機能活性を保証するわけではありません。[3]細胞の種類によって、凍結、融解プロセスへの耐性は様々であり[4]、細胞の種類によって、適切な凍結、融解方法を選択することが重要です。
さらに、凍結保存した製品を融解して患者に直接投与することが可能な一方、全てがこのケースに当てはまるわけではありません。細胞製品の中には、注入の前に洗浄や希釈ステップが必要なものもあり、これらのステップの患者への影響については、時間的な遅れや、追加操作によって起こる生存率の減少を慎重に考慮しなければなりません。
可能ならば、例えば旧medcisionのThawSTAR凍結細胞自動融解ステーションのような自動融解プロセスが、細胞の生存率や回復を改善するのに役立ちます。
生存率や機能の改善に加え、注入時の安全性を確保するためには、医師もまた、一歩前進する必要があります。医療業界において、特に病院や手術室で、治療用の細胞をウォーターバスで融解することは、融解方法として最適ではないのではないかという懸念が大きくなっています。水を使用するシステムは、元来コンタミネーションのリスクを有しており、近年の研究によって、水を使用する加温・冷却デバイスと肺炎菌感染のアウトブレイクについて関連性が認められています。[5,6]そのため、病院でこのデバイスが有するリスクの認識向上を目的とし、FDAはこのデバイスの安全性に関する警告を公表することを決定しました。
ウォーターバスの融解に関する、より厳しい規制ガイドラインが、凍結保存製品に強く依存する細胞産業に影響を与えることは疑いようもありません。水が不要な自動化融解システムは、そういったリスクを有しておらず、細胞療法の下流プロセスに対して安定した要素であり、医師にとっては魅力的な代替品となります。
凍結保存した幹細胞製品のプロセスコントロールが重要だということを認識しているのは、ミラノの臍帯血バンクだけではありません。Center for Innovation and EngineeringのディレクターであるIan Gaudet氏は、細胞療法の開発、製造を行う際、最終製品を凍結保存する上での重要点について発表しています。[7]
Dr. Gaudetは、新しく分離された細胞は開発段階に適しているとする一方で、後期臨床試験や市場製品として使用を検討できないのであれば、それは実践的ではないとしています。患者、製造業者ともにリスクを軽減するということは、つまり、温度感受性の高い製品の輸送や製品の凍結保存、そして、病院における取扱いに関し、厳密な計画を立てるということです。
結局のところ、細胞のポテンシャル発揮に必要な、下流の細胞取扱いプロセスが、細胞療法を産業化する上でしっかりと検討されていないと思います。新しい細胞療法の上市に関しては、科学業界がこの状況に速やかに対処すれば、それが、より良い体制作りにつながることでしょう。
- 参考文献:
-
- [1] Lecchi L., et al. An update on methods for cryopreservation and thawing of hemopoietic stem cells. Transfusion and Apheresis Science. 54: 324–336. 2016.
- [2] Shanley A. Cold Chain: Going the extra Mile. PharmTech.com, 2016.
- [3] Morgenstern D. A., et al., Post-thaw viability of cryopreserved peripheral blood stem cells (PBSC) does not guarantee functional activity: important implications for quality assurance of stem cell transplant programs. British Journal of Haematology. 1-10. 2016.
- [4] Berens, C. et al, Variable resistance to freezing and thawing of CD34-positive stem cells and lymphocyte subpopulations in leukapheresis products. Cytotherapy 18: 1325-1331. 2016.
- [5] Johnson MM, and Odell JA. Nontuberculous Mycobacterium Pulmonary Infections. J. Thorac. Dis. 6(3): 210-220. Mar 2014.
- [6] Sax H., et al. Prolonged outbreak of Mycobacterium chimaera infection after open chest heart surgery. Clinical Infectious Diseases. 2015.
- [7] Gaudet I. The Cold Truth: Cryopreservation of Final Product in Cell Therapy Manufacturing. PCT Pulse. Sept. 2016.
PDFファイルはこちらからダウンロードできます。
記事一覧はこちら

